







《第7章 化学与材料PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为5.04 MB,总共有44页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 44页
- 5.04 MB
- VIP模板
- ppt
- 数字产品不支持退货
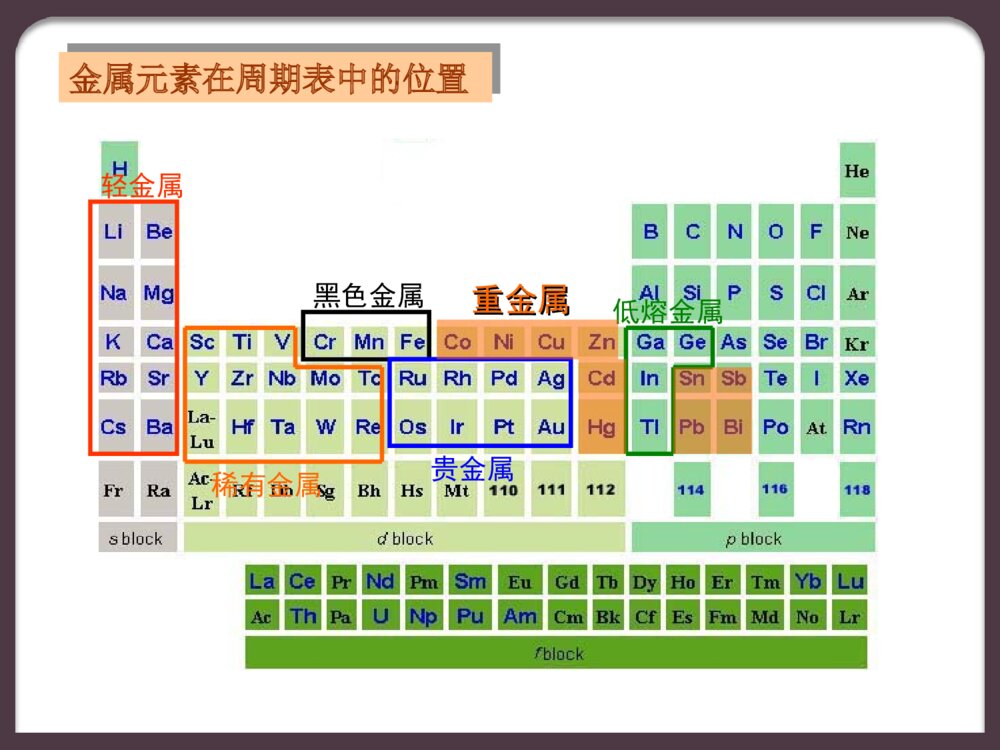
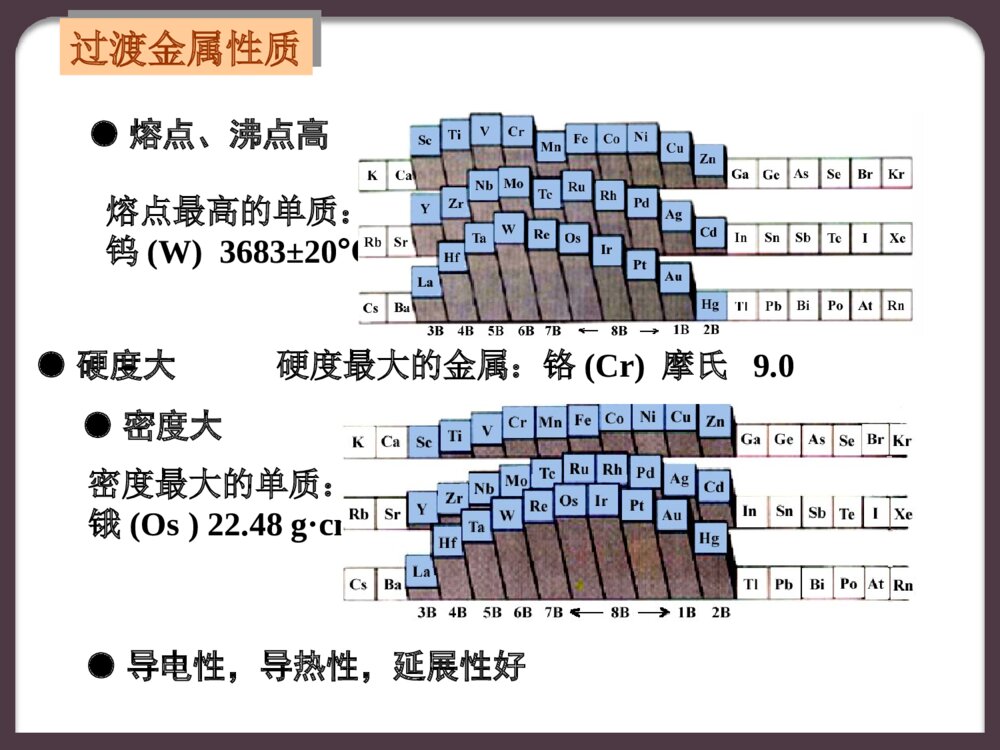
第7章化学与材料Chapter7ChemistryandMaterial本章教学要求了解材料的重要性及目前分类的主要依据;用化学观点理解“材料的性能取决于材料的化学组成和结构”;了解金属存在的形式及钢铁腐蚀与防腐原理;了解常用的无机非金属材料及用途了解高分子化合物的结构特点及分类了解各种新型材料的结构与性能的关系7.1金属材料定义及分类本章教学内容6.了解对角线规则和锂、铍的特殊性.7.2金属的腐蚀与防止7.3特种合金材料7.4常用的无机非金属材料7.4高分子材料7.1金属材料定义及分类金属材料是指由金属元素或以金属元素为主的合金形成的具有一般金属性质的材料合金是由两种或两种以上的金属(或金属和非金属)元素组成的具有金属特性的物质.-3-3黑色金属:铁、铬、锰及其合金轻金属:密度小于5gcm的金属及合金如Na、Ca、Mg、Al稀有金属中的Li、Rb、Cs、Be等.重金属:指密度大于5gcm的金属.铷Cr、Mn、Fe、Co、NiCu、Zn、Cd、Hg、Pb等金属贵金属:化学性质稳定、产量较少、价值较高的金属.如Au有色金属:Ag、Pt、Ir等高熔点金属:主要包括第4、5、6、7(Mn除外)族的元素低熔点金属:熔点较低的金属.Sn、Pb、Bi、Ga、In、Tl稀有金属:自然界中含量很少的金属稀土金属:15种镧系元素和钪、钇元素统称为稀土金属金属的分类金属元素在周期表中的位置轻金属贵金属低熔金属黑色金属稀有金属重金属重金属S区金属性质它们都有金属光泽,密度小,硬度小,熔点低,导电、导热性好的特点.LiNaKRbCsBeMgCaSrBa●硬度大硬度最大的金属:铬(Cr)摩氏9.0●导电性,导热性,延展性好●熔点、沸点高熔点最高的单质:钨(W)3683±20℃●密度大密度最大的单质:锇(Os)22.48g·cm-3过渡金属性质各类金属的用途1.碱金属和碱土金属(s区金属):是化学活泼性最大的金属,是极好的还原剂、脱卤剂。钠汞齐、金属镁在有机合成中有着重要的用途。有些金属,如铯,经过照射后会产生电流,即能产生光电效应。因而铯、钾、铷常被用作光电材料,制成的光电管在科学技术上有重要的应用。2.S区金属及铝属于轻金属:是制造轻质合金的重要原料。铍、镁、铝适于制造轻质合金,其余金属单质都比较软而且太活泼。镁合金、铝合金和铍合金密度小而强度大,是重要的轻型结构材料,广泛应用于宇宙飞船、航空、汽车、机械工业方面。3.碱金属及P区金属单质:大多数熔点低,是制造低熔合金的重要原料,通常用于制造低熔合金的主要为锡、铅、铋等。其中铋是许多重要的低熔合金的主要成分。4.分布于周期表中金属与非金属交界区的一些金属元素,是典型的半导体材料:如镓、铟、锗等,大量用于制造各类半导体器件及电子元件。上世纪七十年代,一些IIIA-VA、IIB-VIA族化合物,如CdSe、GaAs等也被发现又半导体性质。此外,含有这些元素的某些合金,是具有实用价值的超导材料,如Nb3Ge(Tc:23.3k)、Nb3Sm(Tc:18.3k)、V3Ga(Tc:15.4k)。5.银、铜、金、铝是所有金属中导电性最好的。银和金的化学稳定性高,但价格贵,通常在要求较高的场合用作导电元部件,而铜和铝(尤其是铝、质轻价廉)则广泛用于电器工业,制造各种导线、电缆、电极及导电元部件。6.金、银、铜自古以来就是制造货币的主要材料:直至今天仍是一些国家造币合金的成份。此外制造各种饰物,器皿以及精美的工艺品、收藏品也是金和银的一个重要用途。7.铁是所有金属中用途最广、用量最大的一种金属,从远古铁器时代起,铁就是制造生产工具、生活用具和武器的基本材料。今天,铁仍是各种不同性能的钢材的基本成分。铁、钴、镍有顺磁性,它们是许多磁性材料的主要成分。8.铂系金属有很高的化学稳定性,且耐高温。化学工业中用它们制造特殊用途的反应器皿、蒸发皿、坩埚。铂、钌、铑、钯也是制造耐腐蚀电极及热电偶的重要材料。铂铱合金用于制造标准度量衡的校准器,锇铱合金还用于制造指南针的主要零件及自来水笔等。大多数铂系金属能吸收气体,尤其是氢气,其中钯吸收氢气的功能特别强。9.高熔金属钨和铬还是用作金属陶瓷的重要原料。是一种很有用的新型结构材料。此外,钨、钼等高熔金属还常被用作电子仪器中的热电子发射(阴极)材料,稀土在地表中总含量0.0153%稀土资源我国最为丰富,占世界的80%,而且矿藏分布广,从南到北十多个省区均有,品种齐全,内蒙的包头市堪称稀土之城。10.稀土金属:微量稀土金属可大大改善甚至根本改变合金的性质,被称为冶金工业的维生素,是重要的合金成分。在玻璃、陶瓷工业中,稀土元素常作为添加剂。稀土将是磁、光、电等功能材料的最佳载体,稀土金属广泛应用于制造磁性材料、发光材料和原子能材料等方面。稀土元素结构特点和性能:①4f0~4f14独特亚层②大的原子磁矩、各向异性(磁性材料)③丰富的能级跃迁(发光材料)④大范围可变的配位数6~14(材料、生命科学)⑤有序变化的原子和离子半径当金属与周围介质接触时,由于发生化学作用或电化学作用而引起的破坏叫做金属的腐蚀。估计每年腐蚀而报废的钢铁设备相当于钢铁年产量的1/4,发达国家年经济损失占GDP的3~4%。因此在了解金属腐蚀机理的基础上懂得如何防止金属腐蚀和了解如何进行金属材料的化学保护十分必要。金属腐蚀的本质都是金属原子失电子被氧化的过程。7.2金属的腐蚀与防止金属与周围介质直接发生氧化还原反应而引起的腐蚀叫化学腐蚀。1化学腐蚀化学腐蚀发生在非电解质溶液中或干燥的气体中,在腐蚀过程中不产生电流。如:钢铁的高温氧化脱碳、石油或天然气输送管部件的腐蚀等。化学腐蚀原理比较简单,属于一般的氧化还原反应。腐蚀的分类金属与周介质发生电化学作用而引起的金属腐蚀。例如,钢铁在潮湿的环境中生锈,发生的就是电化学腐蚀。2电化学腐蚀E较小的金属易失电子,被氧化而腐蚀,是腐蚀电池的阳极(也称负极)。电化学腐蚀比化学腐蚀普遍得多,腐蚀的速率一般也快得多。①析氢腐蚀在酸性较强的条件下钢铁发生析氢腐蚀,电极反应为:阳极:Fe-2e-=Fe2+阴极:2H++2e-=H2↑在弱酸性或中性条件下钢铁发生吸氧腐蚀,电极反应为:阳极:Fe-2e-=Fe2+阴极:2H2O+O2+4e-=4OH-吸氧腐蚀比析氢腐蚀更为普遍。②吸氧腐蚀1.改变金属的内部结构:例:把铬、镍加入普通钢中制成不锈钢。2.保护层法:例:在金属表面涂漆、电镀或用化学方法形成致密而耐腐蚀的氧化膜等。如白口铁(镀锌铁)、马口铁(镀锡铁)。3.缓蚀剂法:在腐蚀介质中,加入少量能减小腐蚀速率的物质以防止腐蚀的方法。①无机缓蚀剂:在中性或碱性介质中主要采用无机缓蚀剂,如铬酸盐、重铬酸盐、磷酸盐、碳酸氢盐等。主要是在金属的表面形成氧化膜或沉淀物。②有机缓蚀剂:在酸性介质中,一般是含有N、S、O的有机化合物。常用的缓蚀剂有乌洛托品、若丁等。腐蚀的防止4.阴极保护法:将被保护的金属作为腐蚀电池或电解池阴极而不受腐蚀。它一般分为牺牲阳极保护法和外加电流法。牺牲阳极保护法用较活泼的金属或其三元合金如(Zn、Al)连接在被保护的金属上,被保护的金属作为腐蚀电池阴极而达到不遭腐蚀的目的。7.3特种合金材料特种合金是指具有特殊功能,在特殊条件下作结构材料使用的一种合金,如轻质合金、硬质合金、高温合金、低温合金等,虽然使用量较小,但是属于极端条件下不可取代的材料,因此非常重要。轻质铝合金铝的炼制纯铝质软,不耐磨,强度低,不能作结构材料;加入一定量的铜、镁等元素可制得硬铝,主要用作建筑装饰材料等;再加入5%7%的锌可制成被称为超硬铝的铝锌镁铜合金,这种合金硬度高,密度小,易成型,是良好的航空轻质结构材料。随着飞机性能要求的日益提高,提高轻质合金综合性能,并同时降低合金密度是轻质合金的主要发展方向。铝锂合金便是在这样背景下迅速发展的一类新型轻质合金。)()()(冰晶石助熔,熔融电解l3Os4AllOAl2232硬质合金硬质合金是指第4(ⅣB)、5(ⅤB)、6(ⅥB)族的金属和原子半径小的碳、氮、硼形成的间隙合金,这些合金的硬度和熔点特别高,被称为硬质合金,常用于钻头、金属切削工具等的制作。硬质合金是一种主要由不同的碳化物和粘结相组成的粉末冶金产品。主要碳化物有:碳化钨WC、碳化钛TiC、碳化钽TaC、碳化铌NbC在大部分情况下,钴作为粘结相使用。高温合金高温合金是指在600℃1200℃高温下保持较高的强度和韧性并具有抗氧化或抗腐蚀能力的合金。高温合金的基体几乎都是原子扩散能力较小的面心立方结构的奥氏体,可在铁、钴或镍中加入高熔点金属制成。高温合金主要用于制造航空、舰艇和工业用燃气轮机的高温部件,还用于制造航天飞行器、火箭发动机、核反应堆、石油化工设备等。低温合金(1)通常把常温以下直到绝对零度的温度区间称为低温。低温合金指适合在低温下使用而不至产生脆性破坏的合金。一般情况下,合金在低温下会变硬,容易产生脆硬性破坏。著名的泰坦尼克号沉船事件,就是钢在低温下发生脆性破坏的事故之一。由于那时使用的钢含硫量较高,当船在北海冰冷的海水中与冰山相撞后,发生了脆性断裂导致了上世纪最大的海难事故。氮化硅Si3N4组成氮化硅的两种元素的电负性相近,属强共价键结合的原子晶体,所以氮化硅的硬度高(耐磨损)、熔点高(耐高温)、结构稳定、绝缘性能好,故是制造高温燃气轮机的理想材料。缺陷是抗机械冲击强度偏低,容易发生脆性断裂。7.4常用的无机非金属材料耐热高温结构材料氮化硅的合成方法硅氮结合法还原氧化法化学气相法热分解法制成的Si3N4粉体还需要经成型,烧结制成43K15732NSiN2Si3,无氧CO6NSiN2C6SiO34322HCl12NSiNH4SiCl343K167334343423432NH8NSi)NH(Si3NH2NSi)NH(Si3有些物质在特定的温度以下,其导电率将突然增至无穷大,这种现象称为超导电性。Bednorz和Müller因发现La-Ba-Cu-O氧化物(Tc=30K)超导体,荣获1987年诺贝尔物理学奖。目前已发现30种单质,8000余种金属、合金、化合物具有超导性。半导体材料指导电性能介于导体和绝缘体之间的材料J.G.贝德诺兹JohannesG.BednorzK.A.穆勒KarlA.Müller超导材料超导材料1911年,荷兰氦液化器的发明者昂尼斯偶然发现液氦温度(4.2K)下,汞电阻突然消失的现象,由此开始了被称为超导现象的研究。进一步研究表明,要成为超导状态,温度T、磁场强度H和电流密度J都必须分别处于临界温度Tc,临界磁场强度Hc和临界电流密度Jc以下。物质在超导状态下,不仅电阻为零而且其内部的磁感应强度也为零(也就是说是完全性抗磁性的)。超导体的电阻为零意味着电能在产生和输送的过程中将无电阻损耗,这是及其诱人的应用前景之一。然而液氦(4.2K)温度的苛刻使用条件则严格地限制了超导材料的普遍应用。液氮无论在价格、来源、制备还是使用上都比液氦有较大的优势。光导纤维简称光纤,以传光和传像为目的的一种光波传导介质。光导纤维的最大应用是激光通讯,它具有信息容量大、重量轻、抗干扰、保密性好等优点。光导纤维纳米材料纳米科技就是在1-100nm范围内研究原子、分子的结构,通过直接操作和安排原子、分子将其组装成具有特定功能和结构的一门高新技术。纳米材料应用广泛,如美国制成的GaN和ZnO纳米导线,能发出紫外光,这对制造“单片实验室”非常有用。它可用于快速和低成本地分析医学、环境和其他样品。纳米材料纳米碳管1990年,瑞士科学家发现管状结构的碳分子,称为碳纳米管。它由六元环形的碳原子组成的管状大分子,管的直径为零点几到几十纳米,管长为几十纳米到1微米。碳纳米管由几个到几十个单层碳管同轴套构成,相邻管径向间距为0.34nm。碳纳米管有许多优异性能。如强度比钢高100倍,具有优良的导热性和导电性等。7.5高分子材料高分子化合物(macromolecularcompounds)又称高聚物(polymer),其相对分子质量很大,通常大于104,长度在102104nm间甚至更长的分子。尽管高分子化合物的分子很大,其化学组成却往往是比较简单的,一般都是由相同的结构单元重复而成。氯乙稀分子聚合形成聚氯乙烯CH2CH聚合CH2CHnClCln氯乙烯称为单体(monomer),组成高分子链的重复结构单位—CH2–CHCl—称为链节(chain),链节的数目n称为聚合度(degreeofpolymerization)。对同一种高聚物来说,n并不相同,所以高分子化合物的分子量是指平均分子量,即高分子化合物实质上是聚合度不同的分子的混合物。结构特点高分子化合物的形状有线型结构(linearstructure,包括带有支链的)和体型结构(bodilystructure)两种。线型高分子支链型高分子体型高分子柔顺性线型高聚物除了分子链可以运动外,分子链中的C—C单键(σ键)能够围绕相邻单键键轴,保持一定的键角旋转。因此,一个分子链在空间可以有众多变化着的空间形态,且绝大部分呈卷曲状。若作用以外力,分子的形态会发生改变,同时引起物体外形的改变。去除外力,又能借单键的旋转运动而恢复其卷曲状态。高分子链的这种强烈卷曲倾向称为柔顺性(flexibility)。柔顺性越好,高聚物的弹性就越好。热性能(1)高聚物从固态变为液态时,一般没有确定的熔点。对于线型非晶态高聚物而言,随着温度的变化,从固态逐步软化变为液态的过程中,出现三种不同的力学状态,即玻璃态、高弹态和粘流态,它们是分子处于不同运动状态的宏观表现。TgTf温度形变玻璃态高弹态粘流态热性能(2)玻璃态和高弹态间的转变温度称为玻璃化温度,用Tg表示;高弹态与粘流态间的转变温度称为粘流化温度,用Tf表示。人们习惯上把Tg高于室温的高分子化合物称为塑料;把Tg低于室温的高分子化合物称为橡胶;把Tf低于室温,在常温下处于粘流态的高分子化合物称为流动性树脂橡胶的Tg越低,Tf越高,其适用的温度区间越大;塑料则希望其Tg越高,Tg与Tf相差小,稳定而可塑性好体型高分子无粘流态,且Tg很高。弹性弹性是指某物体形变的可恢复性。线型高分子化合物在通常情况下总是处于能量低的卷曲状态。由于分子链的柔顺性,当这种聚合物受到拉力时,卷曲的分子可以被拉直一些。这时分子的能量增高。除去拉力后,又会缩卷起来。这就使物体呈现了弹性。例如,橡胶具有良好的弹性。线型或轻度网型聚合物都有不同程度的弹性,但交联多时会失去链的柔顺性,变成僵硬且弹性差的物质。塑性线型高分子化合物加热至粘流态通过模子压制成形,冷却去压后仍保持其形状的性质叫塑性。塑料就是因为具有可塑性而得名的。反复加热冷却仍保持可塑性的线型高分子化合物称为热塑性高分子化合物,如聚乙烯、聚苯乙烯、聚酰胺等,它们易于加工,可反复应用;另有一些聚合物如酚醛树脂、脲醛树脂在加热过程中会继续起变化,分子链互相交联,结果转变为失去可塑性的体型结构,不能多次加热压模,这类物质称为热固性高分子化合物。机械性能主要是指抗压、抗拉、抗冲击及抗弯曲等,这些性能取决于一下因素:平均聚合度适当增大,可提高拉伸与抗冲击强度,过高不但拉伸强度变化不大,还会使Tf升高而不利于加工;高聚物分子链中含有极性基因或链间形成氢键时,都可增大分子链间的作用力而提高其拉伸强度;适度的交联可提高抗冲击强度,但过分交联则使材料变脆。如乙烯适度交联后,抗冲击强度可提高3~4倍。而酚醛塑料因交联程度高而变脆;绝缘性高分子化合物对电具有良好的绝缘性,这与其结构有关。高分子化合物的分子都是由原子通过共价键结合而成的,分子中没有自由电子和离子,所以不具有离子性或电子性的导电能力。高分子化合物的大分子链呈卷曲状态,互相纠缠在一起,受热、声作用后分子不易振动起来,因而它对热、声也具有绝缘性。化学稳定性高聚物的化学稳定性较高,许多高分子材料可以制成耐酸、碱及其他化学试剂的优良器皿。在某些物理因素(如光、热、高能射线)、化学因素(如水、氧、酸、碱)以及生物因素(霉)的作用下,很多高聚物,也会发生化学变化,这种由于环境的影响使高聚物的性能变坏的现象称为高聚物的老化。在引起高聚物老化的诸因素中,以氧、热、光最为重要,通常又以在光、热等因素的影响和促进下发生氧化而降解的情况为主。为提高高聚物材料的使用价值,可采取改变高聚物结构、加防老剂(稳定剂)及在材料表面镀(或涂)膜等措施以防止老化。



















